有机化学学习笔记——醛酮第一部分
醛酮第一部分
2020.3.20修改
增加了思维导图和目录链接
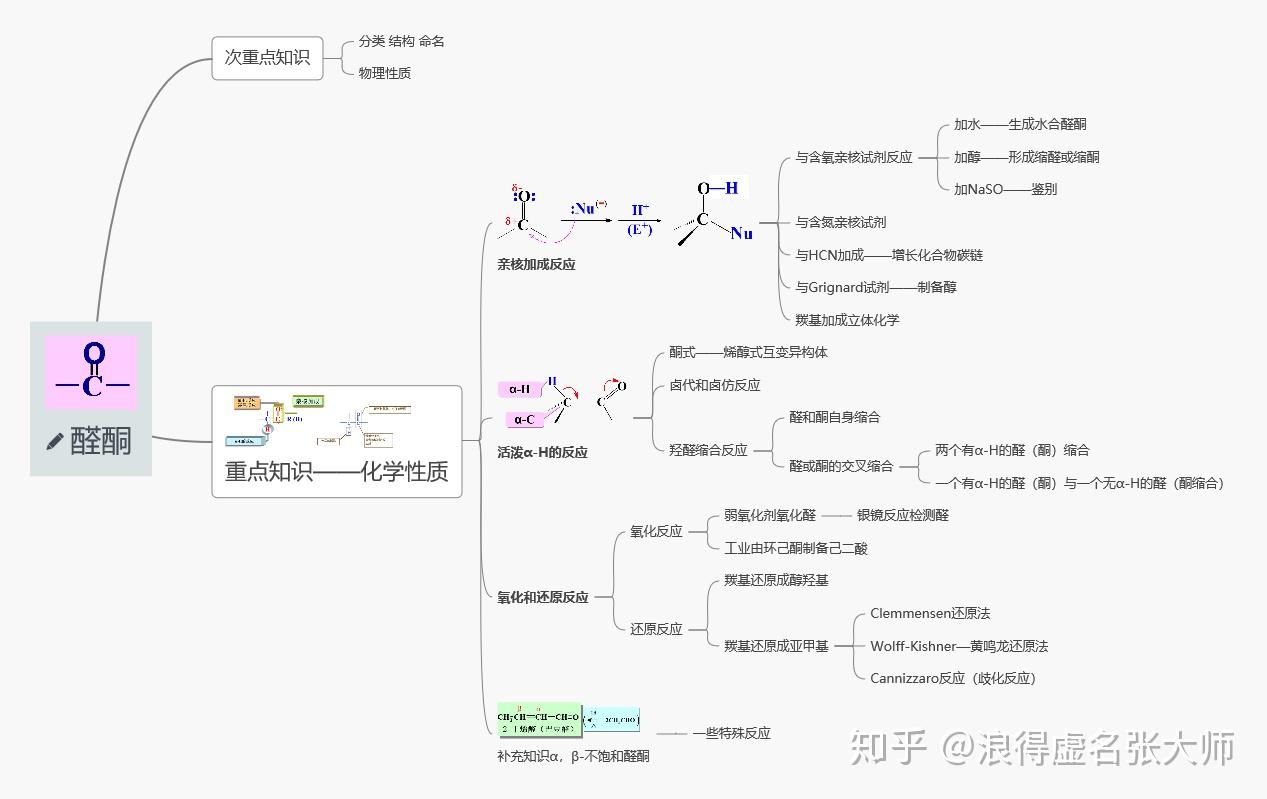
目录链接
浪得虚名张大师:化学学习笔记——目录
参考内容 《有机化学》李艳梅 《有机化学学习指导》东南大学出版社 《有机化学》胡宏纹版 《有机化学》天津大学出版社 课程ppt

这个部分因为整理出的内容也不少,所以第一个部分先整理了相关的概念和亲核加成反应。
内容有需要完善的部分后续还会完善。
写在前面,提到醛酮,不知道大家在大脑里有没有对这两种有机物的相关概念。
脑海中有没有浮现出一种有代表性的醛或者酮呢?
实际上还是需要这样的印象的,因为人总是善于学习熟悉的东西,或者至少说,能够建立起由熟悉的桥梁通往未知。比如学习醇的章节,因为有乙醇这样一个我们日常生活中都能接触到的东西,所以对它概念性质等的理解会深刻很多。
随着有机化学学到后面,可能很多物质离我们的生活没有像乙醇这样常见,也是应该在脑海中构建这样一个典型的物质,来帮助自己理解和记忆。
醛酮的话,最有名的物质,应该就是甲醛了。还有它大名鼎鼎的水溶液——福尔马林。
相信这两个名词,大家都不陌生,一个是大家避之不及的致癌物质,一个是用途广泛的防腐剂。相信这两个名词,大家都不陌生,一个是大家避之不及的致癌物质,一个是用途广泛的防腐剂。
而酮,实验室最常见的就是丙酮。这是一种实验室常用的溶剂。
当然,还有很多酮类物质的药品和毒品等。

例如氯胺酮和卡西酮类。
常被称为K粉和丧尸药。
附加一点禁毒知识,应该算是学习化学者的一点点常识
还有这些毒品的介绍
那么说回正题,我们来看看醛酮的各种性质。那么说回正题,我们来看看醛酮的各种性质。
首先,概念
醛(aldehyde)和酮(ketone)是分子中含有羰基(carbonyl group)官能团的有机物。

结构
醛酮中的碳原子是sp2杂化,而一般认为氧原子没有杂化。碳原子的三个sp2杂化轨道相互对称地分布在一个平面上,其中之一与氧原子的2p轨道在键轴方向重叠构成碳氧σ键。碳原子未杂化的2p轨道垂直于碳原子三个sp2杂化轨道所在的品平面,与氧原子的另一个2p轨道平行重叠,形成Π键,即碳氧双键也是一个由σ键和一个Π键组成。

命名 分类
这个部分按常规省略,命名还是得自己多加练习掌握,很多复杂的结构多写几遍肯定也会了。
邢其毅老师的经典《基础有机化学》中有专门的章节介绍有机化合物的分类 表示方法 命名
各个版本的有机化学书也都有涉及。
如果觉得命名成困难的话,可以先看书,然后在网上寻找一些课程视频。
因为自己看到很多人问关于有机化学的命名问题,有机化合物数不胜数,随便一个都可以拿出来命名,最重要的是掌握方法,多加训练。
物理性质
状态 沸点:醛、酮沸点比相对分子质量相同的烃类高, 比相应的醇低。甲醛在室温下为气体,市售的福尔马林是40%的甲醛水溶液。除甲醛为气体外,12个碳原子一下的脂肪醛酮均为液体。高级脂肪醛酮和芳香酮多为固体。

水溶性:低级的醛酮易溶于水。醛、酮的水溶度比相应的烃或醚大。低级醛酮如甲醛、乙醛、丙酮能与水混溶, 其它醛酮水溶度随相对分子质量增加而下降。
原因:由于这些醛酮可与水分子形成分子间氢键。
化学性质
总述
还是那句话,化学反应,应该根据化学键来进行记忆。
那么首先先把这些内容进行一个汇总
醛酮主要会发生三种反应。第一个部分先集中整理亲核加成反应。
- 亲核加成反应
- 活泼α-H的反应
- 氧化和还原反应

亲核加成反应
解释:
羰基中氧原子的电负性比碳原子大,Π电子云偏向于电负性较大的氧原子,使得氧原子带上部分负电荷,碳原子带上部分正电荷。
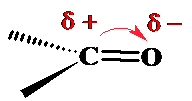
由于氧原子容纳负电荷的能力较碳原子容纳正电荷的能力大,故发生加成反应时,应是亲核试剂(可以是负离子或带有未共用电子对的中性分子)提供一对电子进攻部分带正电荷的羰基碳原子,生成氧负离子。即碳基上加成反应决定反应速度的一步是由亲核试剂进攻引起的,故羰基的加成反应称为亲核加成反应。

- 与含氧亲核试剂反应
- (1)加水--形成水合醛(酮)
水与羰基加成形成醛、酮的水合物。由于H2O的亲核能力比ROH弱, 生成的偕二醇一般是不稳定的, 容易失水, 水的加成反应平衡主要偏向反应物一方。
通式

多数醛酮平衡偏向左边(即1,1-二醇不稳定,易脱水成醛酮),也有些1,1-二醇很稳定,与醛、酮结构有关。

解释
- 取代基电子效应:甲基的超共轭效应使羰基上的正电荷分散,羰基化合物的稳定性也相应提高。
稳定性比较

从反应物看,CH3-为(+I)效应,使羰基中的C的正电荷减少,不利于H2O亲核进攻。
羰基化合物越稳定,水合平衡的位置越偏向左边,即羰基化合物一边。甲醛在水溶液中完全变成水合物,乙醛约有56%变成水合物,而丙酮水溶液中水合物含量极少。
- 取代基的空间效应:羰基碳原子为sp2杂化,∠CCO≈120°,而在水合物中则为sp3杂化,∠CCO≈109°,羰基碳原子上四个基团挤在一起,取代基的体积越大,位阻越大,水合物越不稳定,因此,水合物稳定性为

- 从产物看,CH3-越多,四面体越拥挤,不利于右移,
- 从反应物看,CH3-越多,位阻越大,不利于H2O亲核进攻。
可见取代基的电子效应与空间效应方向一致。
但是,若结构因素使水合物的稳定性相对提高,则使水合平衡偏向右边。
如:
CCl3-CHO生成水合晶体,K[H2O]=2.8×104
C-Cl偶极和C-O偶极互相排斥使羰基化合物稳定性降低,水合平衡相应偏向右边。

- (2)加醇--形成缩醛(或缩酮)
在干燥HCl存在下,醇与醛的羰基加成生成半缩醛,半缩醛还可以与另一分子醇反应, 失水生成缩醛(acetal)。
通式

机理

例子

酮与简单醇不易得到缩酮,但与1,2-二醇能顺利生成环状缩酮。
例子

应用:利用缩醛(酮)的生成和水解来保护羰基

酯与格氏试剂反应可生成三级醇,但酮更活泼,故先得保护酮基。

- (3)加NaHSO3--鉴别
通式

范围:醛、脂肪族甲基酮、低级环酮(C<8)
产物不溶于饱和NaHSO3溶液。以白色浑浊或白色沉淀析出,可用于鉴别。
历程

醛酮的分离、提纯
在产物溶液中加酸或加碱,又回到原来的醛、酮;
此反应常用于分离和精制醛和酮。

- 含氮亲核试剂
与氨的衍生物的加成反应

由于上述N-取代亚胺容易通过结晶进行纯化, 并且又可经酸水解得到原来的醛或酮,所以这些羰基试剂也用于醛、酮的分离及精制。
- 与氢氰酸加成--增长化合物的碳链
反应的范围:醛和脂肪族甲基酮及碳原子数小于8的脂环酮
反应结果:生成α-羟基腈,或称α-氰醇

碱或氰化钠的存在,可以加速醛或酮和氢氰酸的反应;酸的存在则使反应变慢。
作用:这个反应可用于增长化合物的碳链。氰基(-CN)经酸水解可形成羧酸,经还原又可生成胺类化合物。
- 加Grignard试剂 —— 制备醇
醇部分内容入口


Grignard试剂对醛酮的加成是不可逆反应。利用此反应可以制备具有更多碳原子及新碳架的醇。

羰基加成反应的立体化学
当羰基两边的空间条件相同时,亲核试剂从羰基所在平面的上方和下方进攻羰基的几率相等:

实际上还与试剂有关:比如乙醛用氘化铝锂LiAlD4(非手性试剂)还原,的确得到外消旋体。

但苯甲醛用LiAlD(OR)3(手性试剂,其中ROH =

为手性醇)还原,则
(S) >> (R) 即不得到外消旋体,即手性试剂从那面进攻羰基是有选择的,叫对映选择(不对称合成)

当羰基两边的空间条件不同时,亲核试剂更易从位阻较小的一面接近羰基而生成主要产物
例子

总结

文章被以下专栏收录


